百科
硫化氢
概念
H2S的分子结构与H2O相似,呈角形,是一种极性分子,但极性比水弱,不能形成氢键。熔点(-86℃) 和沸点(-71℃)都比水低。
物理性质
H2S是一种无色,有臭鸡蛋气味的气体,比空气稍重,能溶于水(常温常压下,1体积水中能溶解2.6体积硫化氢)。
化学性质
(1)对热较不稳定

(2)强还原性

3.氢硫酸氢硫酸是二元弱酸,可分步电离:
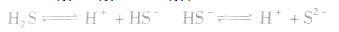
具有挥发性,能使石蕊试液变红。氢硫酸具有酸的通性。
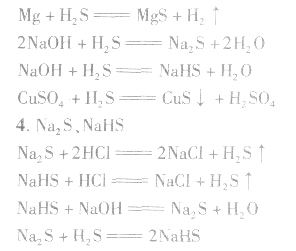
Na2S、NaHS均具有强还原性,在空气中均易被氧化。
S2-遇Fe3+、ClO-、NO3-(H+)等氧化性离子都发生氧化还原反应。
相关试题
A、B、C是短周期里的3种元素的单质,甲、乙是常见的化合物,它们之间存在如图所示的转化关系: 
(1)若A为淡黄绿色气体,用化学式填空:乙是_____________; A、B、C三种元素的原子半径大小为
__________________________
(2)若甲是一种有臭鸡蛋气味的气体,乙常温下为液体,B元素的原子结构示意图为_____________,A+甲的化学反应方程式为:__________________________物质F的水溶液及固体A、D均呈黄色,D是单质,F的溶液遇苯酚显紫色,A是一种重要工业生产中的主要原料。且A、C、D均含有某一非金属元素,C的相对分子质量与过氧化氢的相对分子质量相等。反应过程中生成的水等与转化无关的物质已经略去。这些物质有以下转化关系。试回答以下问题: 
(1)A是___________,C是___________,F是____________(均填化学式)。
(2)A与热盐酸反应的离子方程式为__________________________
(3)写出该框图中由B→E的化学方程式__________________________近期,北京大学的两位教授率先发现人体心肺血管中存在微量硫化氢,它对调节心血管功能具有重要作用。下列叙述正确的是 [ ]
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外电子层都达到8电子结构
C.将硫化氢通入溴水,溴水褪色
D.硫化氢是电解质,其电离方程式是:H2S==2H++S2-元素A的单质能与H2化合生成HxA,在标准状况下 8.5 g HxA气体的体积是5.6 L。含有5.1 g HxA的溶液与
200 mL 0.75 mol/L的CuCl2溶液恰好完全反应,并生成黑色沉淀,则:
(1)A元素的相对原子质量是______,若A的质子数等于中子数,则A是_____元素。
(2)A的最高价氧化物是______,室温下呈______ 态,其分子由____键结合而成。
(3)HxA的电子式为:________。
(4)HxA与CuCl2溶液反应的离子方程式为:____________________。如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。 

试回答下列问题:
(1)实验1中,沉淀最终变为________色,写出沉淀变色的化学方程式_____________________。
(2)实验2甲针筒内的现象有:有________生成,活塞__________移动(填“向外”、“向内”、“不”)。
反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入________溶液中。
(3)实验3中,甲中的30 mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是________,写出NO2与H2O反应的化学方程式________________________。
(4)实验4中,已知:3Cl2+2NH3===N2+6HCl,甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为_____________,最后针筒内剩余气体的体积约为__________mL。已知①2H2S + SO2 == 3S↓+ 2H2O ② S + 2H2SO4(浓)== 3SO2↑+ 2H2O ③ 3S + 6KOH == 2K2S + K2SO3 + 3H2O 则下列说法正确的是 [ ] A.反应①说明能与酸反应,具有碱性氧化物的通性
B.反应②改用稀硫酸,则放出H2
C.反应②和③说明硫具有两性元素的性质
D.上述反应说明硫既有氧化性又有还原性标准状况下H2S和O2混合气体100mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10mL,该10mL气体可能是 [ ]
A.H2S、SO2
B.O2
C.H2S
D.SO3列实验过程中产生的现象与对应的图形相符合的是 [ ] A.NaHSO3粉末加入HNO3溶液中 
B.H2S气体通入氯水中
C.NaOH溶液滴入Ba(HCO3)2溶液中
D.CO2气体通入澄清石灰水中
用FeCl3溶液分别做如下实验,按要求将答案填在空格内。
(1)向其中投入少量金属钠,现象是___,反应的化学方程式是____。
(2)向其中加入过量铁粉,现象是 ____,反应的化学方程式是 ____。将反应后的溶液分装在两支试管中,一支试管中加入氯水,现象是 ____,反应的离子方程式是____ 。另一支试管中加入氢氧化钠溶液,现象是 ____,反应的化学方程式是____。
(3)向其中加入足量的碘化钾淀粉溶液,溶液的颜色呈蓝色,其反应的离子方程式为____ 。
(4)向其中通入硫化氢气体,现象是___ ,反应的离子方程式是___ ,溶液的酸性___。
(5)给FeCl3溶液小心加热至出现红褐色,反应的化学方程式为____。标准状况下,某同学向100mL H2S饱和溶液中通入SO2, 所得溶液pH变化如图所示。下列分析中,正确的是 
[ ]
A.ab 段反应是:SO2 + 2H2S=3S↓+2H2O
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.05mol·L-1
D.b 点对应的溶液导电性最强有a、b、c三种常见的短周期元素,它们之间两两结合构成化合物X、Y、Z,X、Y、Z之间也能相互发生反应。已知X是由a和b元素按原子个数比1:1组成的化合物,a、b、c元素形成的单质(仍用a、b、c表示)和由它们组成的化合物之间的反应关系如下(未配平):
①b+c→Y
②a+c→Z
③X+Y→m
④X+Z→c+n
⑤Y+Z→c+n(1)上述反应中,有最充分理由说明该反应一定属于氧化还原反应的是____(填编号)。
(2)如果m是一种无色黏稠油状液体化合物,则X的化学式是____________。
(3)③反应的化学方程式是________________________________________________。
(4) ⑤反应的化学方程式是________________________________________________。向含0.2mol NaOH的溶液中通入一定量的H2S气体,充分 反应后,将得到溶液小心减压蒸干,得固体7.9g,则该无水物一定含有的物质为 [ ] A.Na2S和NaHS
B.Na2S和NaOH
C.NaHS
D.Na2S向含0.2mol NaOH的溶液中通入一定量的H2S气体,充分 反应后,将得到溶液小心减压蒸干,得固体7.9g,则该无水物一定含有的物质为 [ ] A.Na2S和NaHS
B.Na2S和NaOH
C.NaHS
D.Na2S如图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( ) A.CO2(NaHCO3)溶液/无色喷泉 B.NH3(H2O含酚酞)/红色喷泉 C.H2S(CuSO4溶液)/黑色喷泉 D.HCl(AgNO3溶液)/白色喷泉 
2003年12月23日,川东北某天然气矿井发生特大“井喷”,含有大量硫化氢的天然气逸出,造成243人死亡的重大事故,硫化氢(H2S)是一种无色有臭鸡蛋气味的剧毒气体,可溶于水,有可燃性,完全燃烧生成二氧化硫和水.
请根据以上信息,结合学过的知识,回答下列问题:
(1)事故发生后,若及时采取对逸出气体点火燃烧的措施,可以减少对人员的危害和死亡.写山逸出气体完全燃烧的化学方程:______.
(2)用点燃的方法可除去H2S气体,但生成的二氧化硫又可能造成的危害是______.
(3)专家提醒:发生H2S气体泄漏时,可用湿毛巾捂住鼻子迅速离开现场.这利做法的理由是______.
(4)“井喷”事故发生后,村民虽已闻到弥漫在空气中的臭味,但直到几小时后,村干部通知他们迅速撤离,才意识到危险.对此,你对学习化学知识有何感想:______.为除去混在H2中的H2S气体和水蒸气,得到纯净的H2,应选用的一种物质是( ) A.NaOH溶液 B.CuS04溶液 C.浓H2S04 D.碱石灰 由于易被氧化,在实验室不宜长期保存的溶液是( ) A.Na2SO4溶液 B.NaOH溶液 C.石灰水 D.氢硫酸 已知反应:①2H2S+O2→2S+2H2O
②2H2S+SO2→3S+2H2O
③2H2S+3O2→2SO2+2H2O
将点燃的H2S气体的导管伸入盛有一定量O2的集气瓶内,上述3个反应发生的先后顺序是( )A.①②③ B.③①② C.①③② D.③②① 
如图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( ) A.CO2(NaHCO3)溶液/无色喷泉 B.NH3(H2O含酚酞)/红色喷泉 C.H2S(CuSO4溶液)/黑色喷泉 D.HCl(AgNO3溶液)/白色喷泉 
如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程.该方法对H2S的吸收率达99%以上,并可制取H2和S.下列说法正确的是( ) 
A.吸收H2S的离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+ B.电解过程中的阳极反应主要为:2Cl--2e-=Cl2↑ C.该工艺流程体现绿色化学思想 D.实验室可用点燃充分燃烧的方法消除H2S污染 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
已知:CH4(g)+H2O(g)═CO(g)+3H2 (g)△H=-206.2kJ•mol-1
CH4(g)+CO2 (g)═2CO(g)+2H2 (g)△H=-247.4kJ•mol-1
2H2S(g)═2H2(g)+S2(g)△H=-169.8-1
以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为______.
(1)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是______;燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式:______.
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图1所示.图中A、B表示的物质依次是______.
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图2(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).电解时,阳极的电极反应式为______.
(5)Mg2Cu是一种储氢合金. 350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077).Mg2Cu与H2反应的化学方程式为______.2006年8月下旬科特迪瓦的“毒垃圾”事件造成了严重的环境污染.这些毒垃圾在雨水的浸泡下,散发出类似臭鸡蛋的刺鼻气味,并随雨水流到河流和地下.
(1)据当地科研人员说具有类似臭鸡蛋气味的气体可能就是H2S和溴(化学式为Br2,其性质与氯气相似),如果用CaS表示这些污染物中的硫化物,其与水反应的化学方程式为______.
(2)产生的溴可能是酸性环境中溴Br-和BrO3-发生化学反应而形成,其反应的离子方程式为______.
(3)要消除这些污染物可用______(填试剂的化学式或分子式)溶液来处理.
最新试题
- 1下列叙述正确的是A.由同种元素组成的物质一定属于纯净物B.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物C.元
- 2Do you think people will have robots ?[ ]A. at
- 3A student in our school will be immediately sent home if he
- 4函数,当时,恒成立,则的最大值与最小值之和为( )A.18B.16 C.14D.
- 5古罗马帝国时期的《万民法》规定奴隶在法律上是“可以购买的东西”,宣称保护除奴隶之外的自由民的权利。这说明它
- 665. Wit a large amount of work _______, the chief manager co
- 7大量事实表明,不高于36V的电压才是安全电压。当因出汗或其他因素导致双手潮湿时,人若接触较高的电压,发生危险的可能性
- 8(体验过程题)如图,在4×4的正方形方格中,△ABC和△DEF的顶点都在边长为1的小正方形的顶点上,填空:∠ABC=∠_
- 9美国东部地区和我国东部地区纬度位置及海陆位置大体一致,为什么没有形成显著的季风气候区?_________________
- 10常温下有pH=12的NaOH溶液100mL,要使它的pH为11(体积变化忽略不计)(1)如果加入蒸馏水,应加______
热门考点
- 1如图所示电路中,电源电动势为E、内阻为r,电阻R1、R2为定值电阻,R为滑动变阻器,A、B为电容器的两个极板,电压表和电
- 2(2分)NaOH固体暴露在空气中,容易 ,还能 ,所以需要密封保存。
- 3如图,在△ABC中,BC=4,以点A为圆心,2为半径的⊙A与BC相切于点D,交AB于E,交AC于F,点P是⊙A上一点,且
- 4关于下列实验现象的描述,正确的是( )A.白磷燃烧产生大量白色烟雾B.铁丝燃烧,放出大量热,产生白色火焰,生成一种黑色
- 5能验别伪钞仪器是利用了______能使荧光物质发光的原理.
- 6旦增是七年级(2)班的班长,最近不知怎么的,一遇到烦心事,就忍不住冲别的同学发大火,全班同学也开始讨厌他,你认为雷进同学
- 7A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如右图所示(部分产物略去)。(1) 若A为非金属单质,D
- 82011年9月初开始,广西壮族自治区河池市开展了“民族团结宣传月”活动,利用报纸、广播、电视、手机短信、广告牌、座谈会、
- 9已知椭圆E的中心在坐标原点,焦点在x轴上,离心率为12,且椭圆E上一点到两个焦点距离之和为4;l1,l2是过点P(0,2
- 10下列血管输送的是动脉血的是……………………………………………( )A.上腔静脉B.下腔静脉C.肺静脉D.肺动脉




