百科
电离能
电离能概念
气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量叫做第一电离能。
电离能意义
可以衡量元素的原子在气态时失去一个电子的难易程度。第一电离能数值越小,在气态时原子越容易失去一个电子;第一电离能数值越大,在气态时原子越难失去一个电子。
电离能变化规律
①随核电荷数递增,元素的第一电离能呈周期性变化。
②同一周期内,随着原子序数的增加,原子半径逐渐变小(稀有气体除外),原子核对外层电子的吸引越来越强,元素的原子越来越难失电子,因此元素的第一电离能呈增大的趋势。同一周期内,碱金属元素的第一电离能最小,稀有气体元素的第一电离能最大。
③同一主族,从上到下,随着原子序数的增加,电子层数逐渐增多,原子半径逐渐增大,原子核对外层电子的吸引越来越弱,元素的原子越来越易失电子,故同一主族,随着电子层数的增加,元素的第一电离能逐渐减小。注意通常ⅡA族元素的第一电离能大于ⅢA 族元素、VA族元素的第一电离能大于ⅥA族元素。这是由于ⅡA、VA族元素原子的价电子排布分别为 ns2、ns2np3,是较稳定的全充满或半充满状态,因而失去电子所需的能量较高。
电负性定义
元素相互化合时,原子中用于形成化学键的电子称为键合电子。电负性用来描述不同元素的原子对键合电子吸引力的大小。
电负性意义
电负性越大的原子,对键合电子的吸引力越大。
电负性大小标准
以氟的电负性为4.0作为相对标准。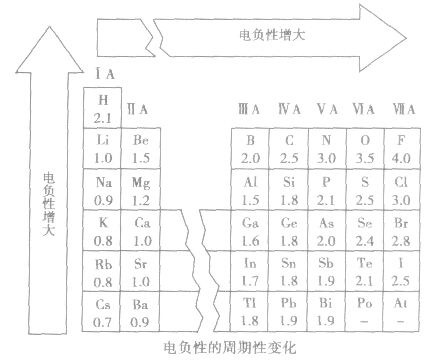
相关试题
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。 
请回答以下问题
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na--Ar元素中,Al的第一电离能的大小(最小)范围为________<Al<_________(填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是______________;
(3)上图中第一电离能最小的元素在周期表中的位置是________________________;
(4)根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有__________性,其中
Be(OH)2显示这种性质的离子方程式是:________________________、_______________________。
(5)单质C不可能具有的性质是___________
A.具有良好的导电性
B.熔沸点很高
C.硬度较小
D.易与Br单质反应,形成的化合物分子是极性分子已知X、Y是主族元素,I为电离能,单位是KJ/mol。根据下表所列数据判断错误的是 
[ ] A.元素X的常见化合价是+1价
B.元素Y是ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。 
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na-Ar之间六种元素用短线连接起来,构成完整的图像。______________________________________
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是_____________________。
(3)上图中6号元素在周期表中的位置是__________;其原子M层电子的轨道表示式为____________。
(4)上图中4,5,6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是
______________________________________。下列关于元素第一电离能的说法不正确的是 [ ] A.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠
B.因同周期元素的原子半径从左到右逐渐减小,故第一电离能必定依次增大
C.最外层电子排布为ns2np6(若只有K层时为1s2)的原子,第一电离能较大
D.对于同一元素而言,原子的逐级电离能越来越大第一电离能I1;________态电_______性基态原子失去________个电子,转化为气态基态正离子所需要的
________叫做第一电离能。第一电离能越大,金属活动性越________。同一元素的第二电离能________第一电离能。比较硼、氮、氧第一电离能大小,并说明理由。
__________________________________________下列说法中正确的是 [ ]
A.第三周期所含的元素中钠的第一电离能最小
B.铝的第一电离能比镁的第一电离能大
C.在所有元素中,氟的第一电离能最大
D.钾的第一电离能比镁的第一电离能大下列关于原子半径和第一电离能的变化趋势的叙述中,正确的是 [ ] A.同周期元素的原子半径随着核电荷数的增大而增大
B.同主族元素的原子半径随着核电荷数的增大而增大
C.同周期元素的第一电离能随着核电荷数的增大而增大
D.同主族元素的第一电离能随着核电荷数的增大而增大下列说法正确的是 [ ] A.第3周期所含的元素中钠的第一电离能最小
B.铝的第一电离能比镁的的第一电离能大
C.在所有元素中,氟的第一电离能最大
D.钾的第一电离能比镁的的第一电离能大元素周期表中前20号元素的第一电离能如图所示。试根据元素在周期表中的位置,分析表中曲线的变化特点,并回答下列问题。 
(1)同主族内不同元素的第一电离能变化的特点是______________________;各主族中第一电离能的这种变化特点体现了元素性质的______________________变化规律。
(2)同周期内,随原子序数增大,第一电离能增大。但个别元素的第一电离能出现反常现象,请分析其反常现象与原子结构的关系,预测下列关系式中正确的是___________(填写编号)
① E(砷)> E(硒) ② E(砷)< E(硒) ③ E(溴)> E(硒) ④ E(溴)< E(硒)
(3)估计Ca 原子的第一电离能[用E(Ca)表示]范围:_______< E(Ca)<________
(4)10号元素第一电离能较大的原因是_____________________________。按原子序数从锂到氟,第一电离能由小到大的次序是____________________。 X与Y两元素的阳离子具有相同的电子层结构,X 元素的阳离子半径大于Y元素的阳离子半径,Y与Z两元素的核外电子层数相同,Z元素的第一电离能大于Y元素的第一电离能,则X、Y、Z的原子序数 [ ] A.X>Y>Z
B.Y>X>Z
C.Z>X>Y
D.Z>Y>X已知电离能是指1 mol气态原子(或阳离子)失去 l mol电子形成了l mol气态阳离子(或更高价阳离子)所需要吸收的能量。现有核电荷数小于20的元素A,其电离能数据如下:(I1表示气态原子失去第一个电子的电离能;In表示离子失去第n个电子的电离能,单位:eV) 
(1)外层电子离核越远,能量越高,电离能越___________(填 “大”或“小”);阳离子电荷数越高,再失去电子时,电离能越___________(填“大”或“小”)。
(2)上述11个电子分属________个电子层。
(3)该元素的主要化合价为_________。
(4)该元素原于的电子排布式为_____________
(5)写出该元素最高价氧化物对应的水化物与稀盐酸反应的离子方程式___________________________。第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。请回答以下问题: 
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na-Ar元素中,Al的第一电离能的大小(最小)范围为 ____< Al<____(填元素符号)。Al的原子最外层电子排布式为_________________。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是_________________________;
(3)上图中第一电离能最小的元素在周期表中的位置是__________________。
(4)根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有___________性,其中Be(OH)2显示这种性质的离子方程式是:_________________________________、____________________________,已知X、Y是主族元素,I为电离能,单位是kJ/mol。根据下表所列数据判断错误的是 
[ ] A.元素X的常见化合价是+1价
B.元素Y是ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应下列关于元素第一电离能的说法不正确的是 [ ] A.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠
B.因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大
C.最外层电子排布为ns2np6(若只有K层时为1s2)的原子,第一电离能较大
D.对于同一元素而言,原子的逐级电离能越来越大下列说法中正确的是 [ ] A.第三周期中所有元素中钠的第一电离能最小
B.硫的第一电离能比磷的第一电离能大
C.在所有元素中,氟的第一电离能最大
D.钾的第一电离能比镁的第一电离能大气态中性原子失去一个电子转化为气态正离子所需要的最低能量叫做第一电离能(I1),气态正离子继续失去电子所需最低能量依次称为第二电离能(I2)、第三电离能(I3)……下表是第三周期部分元素的电离能[单位: eV(电子伏特)]数据。 
下列说法正确的是 [ ] A.甲的金属性比乙强
B.乙的化合价为+1价
C.丙一定为非金属元素
D.丁一定是金属元素电离能是指1mol气态原子(或阳离子)失去1mol电子形成1mol气态阳离子(或更高价阳离子)所需吸收的能量。现有核电荷数小于20的元素A,其电离能数据如下:(I1表示原子失去第1个电子的电离能;
In表示原子失去第n个电子的电离能。单位:eV)
(1)外层电子离核越远,能量越高,电离能越____(填“大”或“小”);阳离子电荷数越高,再失去电子时,电离能越____。(填“大”或“小”)
(2)上述11个电子分属几个电子层?____________
(3)去了11个电子后,该元素还有_______个电子。
(4)该元素最高价氧化物对应水化物的化学式是________。不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。 
(1)同主族内不同元素的E值变化的特点是____________________。各主族中E值的这种变化特点体现了元素性质的____________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系中正确的是
____(填写编号)
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围____<E<____。
(4)10号元素E值较大的原因__________。第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。 
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na~Ar六种元素用短线连接起来,构成完整的图像。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是________。
(3)上图中5号元素在元素周期表中的位置是________、___________。
(4)上图中4、5、6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是
________________________。下列说法正确的是 [ ] A.元素的第一电离能越大,该元素原子越难失去第一个电子
B.同一周期,随着原子序数的增加,元素的第一电离能一定增大
C.同一主族,随着电子层数的增加,元素的第一电离能增大
D.元素的第一电离能不能用来衡量元素非金属性的强弱下列各组元素中,有一组元素原子的第一电离能分别为1086kJ/mol、1402kJ/mol和1313kJ/mol。该组元素 为 [ ] A.C、N、O
B.F、Ne、Na
C.Be、B、C
D.S、Cl、Ar下列关于稀有气体的叙述不正确的是 [ ] A.各原子轨道电子均已填满
B.其原子与同周期IA、ⅡA族阳离子具有相同的核外电子排布
C.化学性质非常不活泼
D.同周期中第一电离能最大下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。 
(1)下列________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
a.原子核对核外电子的吸引力 b.形成稳定结构的倾向。
下表是一些气态原子失去核外不同电子所需的能量(kJ/mol)
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量?__________________________
②表中X可能为以上13种元素中的________(填写字母)元素。用元素符号表示X和j形成化合物的化学式
_______。Y是周期表中____族元素。
③以上13种元素中,____(填写字母)元素原子失去核外第一个电子需要的能量最多。不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如下图所示。试根据元素在周期表中的位置,分析图中吗线的变化特点,并回答下列问题。 
⑴.同主族内不同元素的E值变化的特点是:_____________________。各主族中E值的这种变化特点体现了元素性质的__________变化规律。
⑵.同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常。现试预测下列关系式中正确的是______(填写编号,多选倒扣)
① E(砷)>E(硒)
② E(砷)<E(硒)
③ E(溴)>E(硒)
④ E(溴)<E(硒)
⑶.估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围:________< E <__________。
⑷.10号元素E值较大的原因是___________________。决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示
A通常显____价,A的电负性____ B的电负性(填“>”、“<”或“=”)。
(2)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物
V2O5和CrO2中,适合作录音带磁粉原料的是________________。下列说法不正确的是 [ ] A.元素的第一电离能(I1)是元素的单质失去最外层1个电子所需要吸收的能量,同周期从左到右元素的I1逐渐增大
B.元素的电负性是衡量元素在化合物中吸引电子能力大小的一种标度,同主族从上到下元素的电负性逐渐减小
C.含有阴离子的晶体中一定含有阳离子,含有阳离子的晶体中不一定含有阴离子
D.原子晶体中一定含有共价键;离子晶体中一定含有离子键,可能含有共价键;分子晶体中一定存在分子间作用力已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。根据表中数据封断下列说法中错误的是 
[ ] A.元素X的常见化合价为+1价
B.元素Y是ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能为XCl
D.若元素Y处于第三周期,则它可与冷水剧烈反应下列说法不正确的是 [ ] A.同主族元素,随着电子层数的增加,第一电离能I1逐渐增大
B.同周期元素,随着原子序数的增加,第一电离能I1呈增大趋势
C.通常情况下,电离能I1<I2<I3
D.电离能越小,元素的金属性越强气态原子生成+1价气态阳离子所需要的能量称为第一电离能。元素的第一电离能是衡量元素金属性强弱的一种尺度。下列有关说法正确的是 [ ]
A.元素的第一电离能越大,其金属性越强
B.元素的第一电离能越小,其金属性越强
C.金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关
D.同周期元素,第一电离能随原子序数增大逐渐增大下表为长式周期表的一部分,其中的编号代表对应的元素。 请回答下列问题: 
(1)表中属于d区的元素是____(填编号)。
(2)科学发现,②④⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如下图(图中②④⑨,则该化合物的化学式为____(按 顺序,用元素符号表示)。
顺序,用元素符号表示)。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为____;该元素与元素①形成的分子X构型为____,X在①与③形成的分子Y中的溶解度很大,其主要原因是____。
(4)下表列出了常见元素A~F的第一到第五电离能的数据。
请回答:表中的金属元素是____(填字母),其中化合价为+3价的是____(填字母);若A、B、C依次为同周期相邻元素,表中显示B比A和C的第一电离能都略大,其原因是__________。
已知X、Y是主族元素,I为电离能,单位是kJ/mol。根据下表所列数据判断错误的是 
[ ]
A.元素X的常见化合价是+1价
B.元素Y是ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X原子核外电子层数等于最外层电子数,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第____周期第____族。W的气态氢化物稳定性比H2O(g)____(填“强”或“弱”)。
(2)Y的原子核外电子排布示意图是____,Y的第一电离能比X的___(填“大”或“小”)。
最新试题
- 1曹雪芹著《红楼梦》的主要社会条件是 [ ]A、资本主义萌芽 B、封建制度衰落 C、中国古代文化的影响 D、家
- 2下图AB之间为陆地,读下图完成下列各题。小题1:关于A国说法正确的是A.经济发达,工业以重工业为主B.国土面积大,国内运
- 3The tower on the top of the hill ________ the beauty of the
- 4(6分)有下列晶体:①冰②金刚石③氩④过氧化钠⑤二氧化硅⑥氯化镁⑦纯醋酸⑧白磷⑨氯化铵⑩金属铝。用序号回答下列问题:(1
- 5如图,等腰三角形ABC中,腰AB的垂直平分线MN交另一腰BC于点G,AB=10,△AGC周长等于17,则底边AC的长为[
- 6如果两个相似三角形对应高的比是3:2,那么它们的面积比是______.
- 7我市拥有“三江六岸”的美丽景观和丰富的水资源.为保护水资源,下列做法可取的是[ ]A.大量使用含磷洗衣粉 B.合
- 8化简求值:(x2+3x)(x-3)-x(x-2)2+(-x-y)(y-x),其中x=3,y=-2.
- 9在下面每句话空缺处依次填入成语,最恰当的一组是(3分)①肖邦之家黄昏时的簌簌声,芬芳的香味,使我们心荡神驰,犹如是在聚精
- 10下图为肺的内部结构示意图,图中所示肺泡外包围着毛细血管,肺泡壁和毛细血管壁都很薄,由一层上皮细胞构成,这有利于 [
热门考点
- 1若对任意,,则实数的取值范围是
- 2作匀加速直线运动的物体,先后经过A、B两点时,速度分别为v和7v,则通过A、B中间时刻的速度是______,如果物体通过
- 3 历史老师布置了一道作业题:中共十一届三中全会即将召开,请你为***拟一份发言提纲。以下刘辉同学所拟提纲中不
- 4如果从原点为圆心的圆经过双曲线的焦点,并且被直线(为双曲线的半焦距)分成弧长为2:1的两段弧,则该双曲线的离心率为(
- 5在Rt△ABC中,∠C=90°,斜边c=5,两直角边的长a,b是关于x的一元二次方程x2-mx+2m-2=0的两个根,求
- 6在比例尺为1:25000000的地图上,1厘米代表的实地距离是[ ]A.25千米 B.2.5千米 C.250千
- 7咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示,下列叙述不正确的是( )A.咖啡鞣酸与浓溴水既能发生取代反应又能发生
- 8关于图中的两类滑轮甲和乙,下列说法正确的是( )A.甲能改变拉力的方向B.甲比乙省功C.甲比乙省力D.甲比乙效率高
- 9Does he like English _____ Japanese? [ ]A. and B. or
- 10三角形三边长分别是㎝、㎝、㎝,则它的周长是( )。



